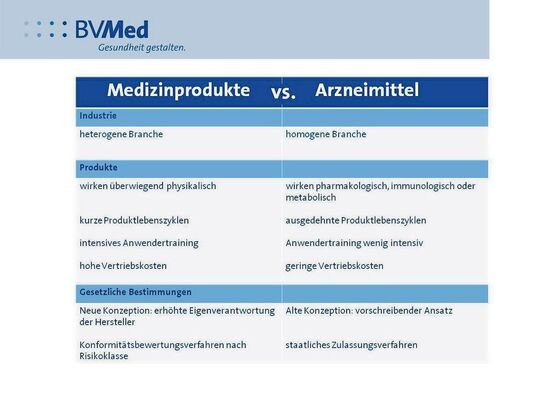
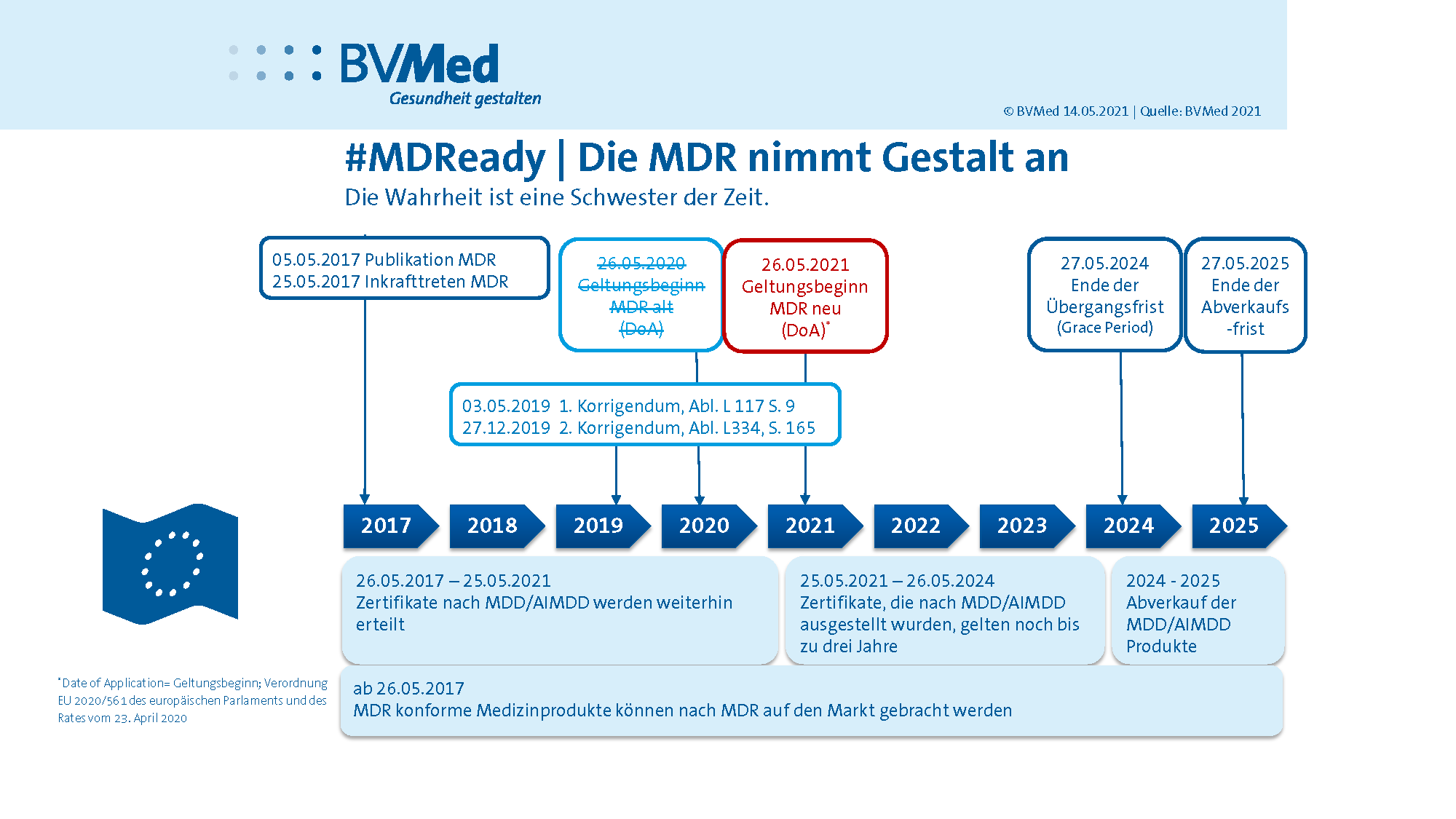
Die Medizinprodukte-Verordnung (MPV) regelte die Bewertung und Feststellung der Übereinstimmung von Medizinprodukten mit den Grundlegenden Anforderungen gemäß § 7 des Medizinproduktegesetzes (MPG) (Konformitätsbewertung), die Sonderverfahren für Systeme und Behandlungseinheiten und die Änderung der Klassifizierung von Medizinprodukten in Deutschland. Die Verordnung trat am 26. Mai 2021 außer Kraft.
Von der deutschen MPV abzugrenzen ist die Medizinprodukte-Verordnung der EU.
Inhalt der Verordnung
- Abschnitt 1 Anwendungsbereich und Allgemeine Anforderungen an die Konformitätsbewertung
- § 1 Anwendungsbereich
- § 2 Biologische Sicherheitsprüfung
- § 3 Allgemeine Vorschriften zur Durchführung der Konformitätsbewertung
- Abschnitt 2 Anforderungen an die Verfahren der Konformitätsbewertung
- § 4 Konformitätsbewertungsverfahren für aktive implantierbare Medizinprodukte
- § 5 Konformitätsbewertungsverfahren für In-vitro-Diagnostika
- § 6 Konformitätsbewertungsverfahren für unter Verwendung von tierischem Gewebe hergestellte Medizinprodukte
- § 7 Konformitätsbewertungsverfahren für die sonstigen Medizinprodukte
- Abschnitt 3 Änderungen der Klassifizierung von Medizinprodukten
- § 8 Brustimplantate
- § 9 Gelenkersatz für Hüfte, Knie und Schulter
- Abschnitt 4 Übergangsbestimmungen
- § 10 Übergangsbestimmung für unter Verwendung von tierischem Gewebe hergestellte Medizinprodukte
- § 11 Übergangsbestimmungen für Gelenkersatz für Hüfte, Knie und Schulte
Weblinks
- Text der Medizinprodukte-Verordnung